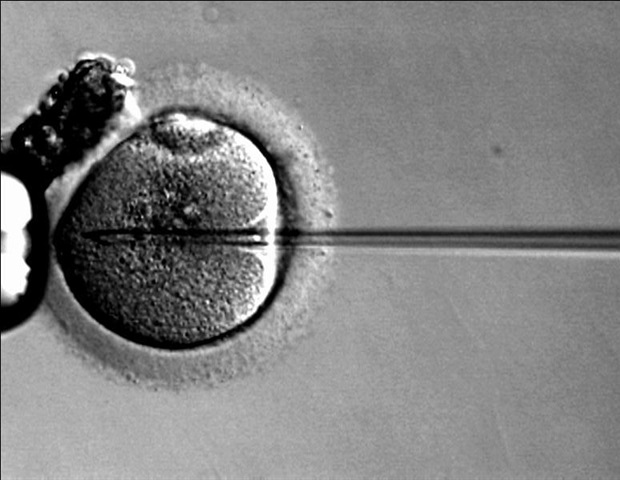
Πειραματική γονιδιακή θεραπεία αποκαθιστά τη λειτουργία του ανοσοποιητικού συστήματος σε παιδιά με γενετική διαταραχή
Μια καινοτόμος γονιδιακή θεραπεία που αναπτύχθηκε από ερευνητές του UCLA, του University College London και του Great Ormond Street Hospital έχει αποκαταστήσει και διατηρήσει τη λειτουργία του ανοσοποιητικού συστήματος σε 59 από τους 62 παιδιούς που γεννήθηκαν με ADA-SCID, μια σπάνια και θανατηφόρα γενετική διαταραχή του ανοσοποιητικού.
Τι είναι το ADA-SCID;
Η σοβαρή συνδυασμένη ανοσοανεπάρκεια λόγω ανεπάρκειας αδενοσίνης δεαμινάσης (ADA-SCID) προκαλείται από μεταλλάξεις στο γονίδιο ADA, το οποίο δημιουργεί ένα ένζυμο απαραίτητο για τη λειτουργία του ανοσοποιητικού. Για τα παιδιά με αυτή την κατάσταση, καθημερινές δραστηριότητες όπως το σχολείο ή το παιχνίδι με φίλους μπορεί να οδηγήσουν σε επικίνδυνες, απειλητικές για τη ζωή λοιμώξεις. Χωρίς θεραπεία, το ADA-SCID μπορεί να είναι θανατηφόρο μέσα στα πρώτα δύο χρόνια της ζωής.
Η νέα θεραπεία και τα αποτελέσματά της
Οι τρέχουσες τυπικές θεραπείες, όπως η μεταμόσχευση μυελού των οστών από συμβατό δότη ή εβδομαδιαίες ενέσεις ενζύμου, έχουν περιορισμούς και πιθανούς μακροπρόθεσμους κινδύνους. Η πειραματική γονιδιακή θεραπεία προσφέρει μια νέα προσέγγιση. Οι γιατροί συλλέγουν τα βλαστοκύτταρα του αίματος ενός παιδιού, τα οποία δημιουργούν όλους τους τύπους αιματικών και ανοσοποιητικών κυττάρων, και χρησιμοποιούν έναν τροποποιημένο ιό lentivirus για να παραδώσουν μια υγιή αντίγραφο του γονιδίου ADA. Αφού επαναχρησιμοποιηθούν στον ασθενή, τα διορθωμένα βλαστοκύτταρα αρχίζουν να παράγουν υγιή ανοσοποιητικά κύτταρα ικανά να καταπολεμούν λοιμώξεις. Η ανάπτυξη των ανοσοποιητικών κυττάρων ξεκινά σύντομα μετά την επαναφορά των τροποποιημένων βλαστοκυττάρων, αλλά χρειάζονται έξι έως 12 μήνες για να επανασταθεί το ανοσοποιητικό σύστημα σε φυσιολογικά επίπεδα.
Σε μια μελέτη που δημοσιεύθηκε σήμερα στο New England Journal of Medicine, ο ανώτερος συγγραφέας Δρ. Donald Kohn από το UCLA και οι συνεργάτες του αναφέρουν μακροχρόνια αποτελέσματα για παιδιά που υποβλήθηκαν στη γονιδιακή θεραπεία μεταξύ 2012 και 2019. Αυτά τα αποτελέσματα είναι ακριβώς όσα ελπίζαμε όταν ξεκινήσαμε την ανάπτυξη αυτής της προσέγγισης. Η ανθεκτικότητα της ανοσοποιητικής λειτουργίας, η συνέπεια με την πάροδο του χρόνου και το συνεχιζόμενο προφίλ ασφάλειας είναι όλα εξαιρετικά ενθαρρυντικά.
Η έρευνα χρηματοδοτήθηκε από τα Εθνικά Ινστιτούτα Υγείας, το Υπουργείο Υγείας και Ανθρωπίνων Υπηρεσιών των Η.Π.Α., το Ινστιτούτο Αναγεννητικής Ιατρικής της Καλιφόρνιας, την Orchard Therapeutics και το Εθνικό Ινστιτούτο Υγείας και Έρευνας της Μεγάλης Βρετανίας. Η μελέτη αυτή αντιπροσωπεύει την μεγαλύτερη και πιο μακροχρόνια παρακολούθηση γονιδιακής θεραπείας αυτού του είδους μέχρι σήμερα, με 474 συνολικά χρόνια παρακολούθησης ασθενών, συμπεριλαμβανομένων πέντε ασθενών που έλαβαν τη θεραπεία πριν από περισσότερα από δέκα χρόνια.
Για τους 59 ασθενείς που θεραπεύτηκαν με επιτυχία, η ανοσοποιητική λειτουργία παρέμεινε σταθερή πέρα από την αρχική περίοδο ανάρρωσης, χωρίς αναφερόμενες επιπλοκές που να περιορίζουν τη θεραπεία. Ο Δρ. Kohn δήλωσε: “Το πιο αξιοσημείωτο είναι ότι όλα έχουν παραμείνει εντελώς σταθερά πέρα από την αρχική περίοδο ανάρρωσης τριών έως έξι μηνών.” Οι περισσότερες ανεπιθύμητες ενέργειες ήταν ήπιες ή μέτριες και σχετίζονταν με τις ρουτίνες προετοιμασίας αντί για τη γονιδιακή θεραπεία αυτή καθαυτή.
Η θεραπεία ήταν επιτυχής σε όλους εκτός από τρία από τα 62 περιστατικά, και όλα αυτά τα παιδιά μπόρεσαν να επιστρέψουν στις τρέχουσες τυπικές θεραπείες. Δύο από αυτούς τους ασθενείς προχώρησαν σε μεταμοσχεύσεις μυελού των οστών και ένας λάμβανε ενέσεις ενζύμου ADA ενώ προετοιμαζόταν για μεταμόσχευση κατά την ημερομηνία κοπής των δεδομένων.
Περισσότερα από τα μισά από τα παιδιά που θεραπεύτηκαν έλαβαν μια κατεψυγμένη προετοιμασία διορθωμένων βλαστοκυττάρων. Αυτά τα παιδιά παρουσίασαν παρόμοια αποτελέσματα με εκείνα που έλαβαν βλαστοκύτταρα που δεν είχαν καταψυχθεί. Η επιτυχία της μεθόδου κρυοσυντήρησης έχει σημαντικές επιπτώσεις για την προσβασιμότητα της θεραπείας σε ασθενείς παγκοσμίως. “Η προσέγγιση της κατάψυξης επιτρέπει στα παιδιά με ADA-SCID να συλλέγουν τα βλαστοκύτταρά τους τοπικά, να επεξεργάζονται και να αποστέλλονται σε άλλο εργοστάσιο και να επιστρέφουν σε ένα νοσοκομείο.